硒
| 本条目部分链接不符合格式手冊規範。跨語言链接及章節標題等處的链接可能需要清理。(2015年12月11日) |
| 本元素尚未参照元素專題之格式編寫。 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 外觀 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 硒的两种同素异形体 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 概況 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 名稱·符號·序數 | 硒(Selenium)·Se·34 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 元素類別 | 非金屬 有人認為其為類金屬 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
族·週期·區 | 16 ·4·p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 標準原子質量 | 78.971(8) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子排布 | [氩] 3d10 4s2 4p4  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 歷史 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 發現 | 贝采里乌斯 和 约翰·甘恩(1817年) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 分離 | 贝采里乌斯 和 约翰·甘恩(1817年) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物理性質 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物態 | 固體 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 | (接近室温) (灰硒) 4.81 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 | (接近室温) (红硒) 4.39 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 | (接近室温) (晶体硒) 4.28 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
熔點時液體密度 | 3.99 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔點 | 494 K,221 °C,430 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 沸點 | 958 K,685 °C,1265 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 臨界點 | 1766 K,27.2 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔化熱 | (灰硒) 6.69 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 汽化熱 | 95.48 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 比熱容 | 25.363 J·mol−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
蒸氣壓
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子性質 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 氧化態 | 6, 4, 2, 1, -2 (强酸性) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電負性 | 2.55(鲍林标度) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電離能 | 第一:941.0 kJ·mol−1 第三:2973.7 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子半徑 | 120 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 共價半徑 | 120±4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 范德華半徑 | 190 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 雜項 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 晶體結構 | 六方 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 磁序 | 抗磁性 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熱導率 | (无定形硒) 0.519 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 膨脹係數 | (25 °C)(无定形硒) 37 µm·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
聲速(細棒) | (20 °C)3350 m·s−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 楊氏模量 | 10 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 剪切模量 | 3.7 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 體積模量 | 8.3 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 泊松比 | 0.33 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 莫氏硬度 | 2.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 布氏硬度 | 736 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS號 | 7782-49-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 最穩定同位素 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
主条目:硒的同位素
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
硒是化学元素,化学符号是Se,原子序数是34,是非金属。
硒對生物來說是必需,但同時也有毒性。硒的性质与硫及碲相似;在有光时,导电性能较黑暗时好,故可用来做光电池。
目录
1 歷史
2 性质
2.1 化学性质
3 對人體的影響
3.1 含量與分佈
3.2 食物來源
3.3 建議量
3.4 對硒的特殊需求者
3.5 吸收
3.6 運輸
3.7 代謝
3.8 生化功能
3.9 硒蛋白生合成分子機制
3.10 缺乏與毒性
3.10.1 缺乏症候群
3.10.2 毒性
3.11 與其他營養素的關係
4 有機硒化學
4.1 硒醇
4.2 硒醚
5 参阅
6 参考文献
7 外部链接
歷史
硒之英文全名為Selenium,取自希臘文Σελήνη(月亮女神塞勒涅的名字),为月亮之意。因為它是一種固體非金屬,故此用石字部首,並賦予西字音譯。
會如此命名,是因為在採礦中,硒(Selenium)總是和元素碲的混雜在一起。先發現的碲(Tellurium)是以拉丁文的地球(Tellus)來命名的。

灰黑色的硒粉
性质
化学性质
硒可以和硝酸或硫酸反应。硒可以在空气中燃烧,产生二氧化硒,伴有蓝色火焰。
硒也可以和大多数金属反应,如[1]:
- Se + Cu —Δ→ CuSe
- Se + 2 Ag —Δ→ Ag2Se
- Se + Zn —Δ→ ZnSe
- 3 Se + 2 Al —Δ→ Al2Se3
- Se + 2 K —液氨→ K2Se
硒和碱金属氰化物共熔,得到硒氰酸盐,如[1]:
- KCN + Se → KSeCN
和过渡金属氰化物在液氨中反应,会有不同的反应发生,如[1]:
- 3 Se + 2 CuCN → Cu(SeCN)2 + CuSe
- 22 Se + 12 AgCN + 16 NH3 → 6 Ag2Se + Se4N4 + 12 NH4SeCN
對人體的影響
硒是人體必需的微量礦物質營養素[2],多以氧化態Se(Ⅱ)、Se(Ⅳ)、和Se(Ⅵ)存在,化學性質與硫相似,許多含硫胺基酸,如甲硫胺酸(Met)、半胱氨酸(Cys)、胱氨酸也可用硒取代硫。
硒在動物組織中最常以硒甲硫氨酸(selenomethionine,簡稱SeMet)和硒半胱氨酸(selenocysteine,簡稱SeCys)的形態存在,其中甲硒胺酸無法由人體合成,僅能由植物合成後經攝食再經消化代謝而獲得,故食材動植物來源組成將決定硒在飲食中的形式,此外,人體中甲硒胺酸可以取代甲硫胺酸;但硒半胱胺酸不能取代半胱胺酸。硒在生理上的功能除了抗氧化外,還調控了甲狀腺的代謝和維他命C的氧化還原態,也曾被提出和抗癌相關的可能性。在食材成分含量裡,同種植物性食材含硒成分變化相當大,乃因各原植物生長地的土壤中硒的濃度不同,當地的動物也隨之反映相應情形,因此硒營養缺乏或過量情形常有地域性關係。
然而,純硒元素和金屬硒化物的毒性相對上不大,而且有些為重要的微量元素之一。嚴重缺乏可引致克山症和溪山症。它們的病徵有:心肌壞死、萎縮、軟骨組織壞死。另外又與甲狀腺腫、呆小症和習慣性流產有關。
含量與分佈
人體本身的硒總含量為15mg。男性體內的硒多集中在睪丸及前列腺輸精管中,會隨精液一起排出體外。人體與動物有二個硒儲存庫,一為身體蛋白質的硒甲硫氨酸(SeMet),它的儲存量視飲食中SeMet量而定,其提供硒的量,取決於甲硫胺酸的轉換率;二為肝臟酵素谷胱甘肽过氧化物酶(glutathione peroxidase,GPX)的硒。
食物來源
硒存在於土壤中,而世界各地的土壤硒含量皆不相同,各地植物所含的硒濃度也因此不同。一般而言,食物中的瘦肉、柿子、蒜頭、海產、蔥、南瓜等含有多量的硒。動物製品的硒含量(約0.4-1.5μg/g)比植物體高;一般植物穀類的硒含量範圍可在<0.1μg/g─>0.8μg/g;在海洋生物中,硒類的含量也比植物多,但由於魚類(尤其是體內含汞的魚類)會形成汞─硒複合體,造成對硒的生物利用性極低,故雖然硒在魚類的含量多但對於魚類本身的利用性極低;至於肉類會提供0.1-0.4μg/g;乳製品的硒含量則為<0.3μg/g。
另外,全穀物和核果種子也是好的來源。在飲水中提供的硒攝取量十分有限,除非水流經含硒量高的土壤地區才可能有較高的含量。
植物中的硒是因硒取代硫而進入植物體,硒型態有甲硒胺酸、硒胺酸與其代謝產物等。動物生長需要硒,在攝食植物時獲得甲硒胺酸。飲食中硒的形式取決於動植物食品的組合。
| 食品名稱/重量 | 硒(μg) |
| 鮪魚 / 3 oz | 68 |
| 火腿(瘦肉)/ 3 oz | 42 |
| 蛤蜊 / 3 oz | 41 |
| 鮭魚 / 3 oz | 40 |
| 義大利蛋麵 /1杯 | 35 |
| 沙朗牛排 / 3 oz | 28 |
| 雞胸肉 / 3 oz | 20 |
| Special K cereal | 17 |
| 麩燕麥片 / 1杯 | 14 |
| 全麥麵包 / 1片 | 10 |
| 燕麥糊 / 1/2杯 | 10 |
| 白麵包 / 1片 | 9 |
| 葡萄乾麥片 / 1杯 | 4 |
建議量
民眾的實際硒攝取量會因地而異,美國平均每日81μg、加拿大每日113–220μg ,高於RDA。均飲食估計可提供約104-124 μg的硒。成人之上限攝取量(UL)訂為400μg。
硒的建議量在1980年只能根據估計而得,稱為Estimated safe and adequate dietary intake(ESADDI);2000年則根據需要量之科學研究而訂定每日建議攝取量(RDA)。
過去曾有關於臺灣境內硒之飲食攝取量的研究[4],分析結果六日飲食的硒攝取範圍在104~124μg(1.3~1.6μmol)/day,平均值為112μg(1.4μmol)/day,加上臺灣非低硒區域,且食品貿易進出口抹去食品在硒含量上的地域性限制,推測臺灣境內應無硒營養缺乏的問題。
- 硒的營養來源:
- 有機型式:甲硒胺酸(selenomethione)、硒半胱胺酸(selenocysteine)
- 無機型式:硒酸鹽(selenate)、亞硒酸鹽(selenite )
- 影響硒營養需求量的因素[5]
- 1.生物吸收率:見「吸收」。
- 2.性別:早期來自中國研究報告,當時硒缺乏現象比現在嚴重,在此情形顯示產齡女性較易罹患克山病(Keshan disease);另外,過去20年報告顯示孩童不論男女有相同的比例罹患克山病;性別的影響必須在硒攝取量極低的情下才會顯現,假設考慮女性有較高機率罹患克山病,硒對各年齡層的需求量將以男性參考體重為基準。
| 年齡 | 美國 (μg/day)[6] | 台灣 (μg/day)[7] | |
| 0 個月~ | AI=15 | 15 | |
| 6個月~ | AI=20 | 20 | |
| 1歲~ | 20 | 20 | |
| 4歲~ | 30 | 25 | |
| 7歲~ | 30 | 30 | |
| 10歲~ | 40 | 40 | |
| 13歲~ | 40 | 50 | |
| 14歲~ | 55 | 50 | |
| 孕婦 | 60 | 60 | |
| 哺乳 | 70 | 70 |
- RDA(建議攝取量 Recommanded Dietary Allowances):美國原始的飲食標準,代表同年齡層中,97~98%人的營養需求量。
- AI(足夠攝取量 Adequate Intake):未能有足夠的實驗資訊建立EAR的情形下,所推估維持健康狀態的量,常用在一歲以下的嬰兒。
| 年齡 | 美國 (μg)[8] | 台灣 (μg)[9] | |
| 0月~ | 45 | 35 | |
| 3月~ | 45 | 50 | |
| 6月~ | 60 | 60 | |
| 9月~ | 60 | 65 | |
| 1歲~ | 90 | 90 | |
| 4歲~ | 150 | 135 | |
| 7歲~ | 150(4~8歲) | 185 | |
| 10歲~ | 280 | 280 | |
| 13歲~ | 400(14歲~) | 360 | |
| 16歲~ | 400 | 400 | |
| 19歲~ | 400 | 400 | |
| 懷孕期 | 400 | 400 | |
| 哺乳期 | 400 | 400 |
- UL(Tolerable Upper Intake Level 上限攝取量):對於97~98%的人不可能產生不良健康影響之每日最大營養攝取量
對硒的特殊需求者
- 以全靜脈注射營養(TPN,Total Parenteral Nutrition)為唯一營養來源者,需要硒的營養補充劑。
- 有嚴重腸胃道疾病(例如:克隆氏症)或曾移去一大段小腸者有硒營養缺乏的風險。
- 碘營養缺乏者。研究指出硒缺乏會惡化碘缺乏的症狀,適當補充硒可以緩解碘缺乏症狀以及在神經系統的影響。
- 使用化療藥物者需要硒營養的補充。有研究指出,多種型態的硒可以減少化療藥物(例如:順鉑,cisplatin)所引發腎和骨髓的傷害。
資料來源:[10]
吸收
有機和無機形式的硒都可以很有效率的被吸收,只是發生在不同的腸道部位;吸收率並非調控動物體硒之恆態的機制。十二指腸是硒主要的吸收位置,空腸和迴腸則有少量的吸收,但胃則沒有吸收硒之能力。甲硒胺酸的吸收效率比亞硒酸鹽(selenite)來的好。含有硒的胺基酸吸收是利用胺基酸運送系統,吸收率可達到80%。甲硒胺酸的吸收率比硒胺酸好。在某些研究中亞硒酸鹽的吸收率可達到85%以上,因與腸道中物質的交互作用,吸收率較有變化。一旦吸收後,保留程度高於硒酸鹽。硒酸鹽(selenate)的吸收又比亞硒酸鹽好,幾乎被完全吸收;但併入組織前,大部分會由尿中排除。
維生素A、維生素C、維生素E都會增加硒的吸收,當在小腸腔的榖胱甘肽(glutathione, GSH)濃度低時也會增加吸收。重金屬(例:水銀)和植酸被認為會抑制硒的吸收。
高劑量的維生素C、鋅及重金屬(例如:汞)會減少硒的吸收;但若在飲食中合併食用硒及維生素C,硒可以和飲食中的胺基酸形成保護結構進而不影響其吸收[11]。
運輸
小腸吸收之硒會和運輸蛋白結合經血液攜帶至肝和其他組織。腎臟、肝臟、心臟、胰臟和肌肉都是硒含量較高的組織,肺臟、腦部、骨骼和紅血球也含有硒。目前如何調控硒從組織釋放到血漿裡或是組織從血漿裡吸收的作用機制仍然不明。存在血漿中的硒,與許多不同分子結合成不同的形式存在著。其中最多的就是硒半胱氨酸(Selenocysteine,Sec):由硒原子取代原本在半胱氨酸中的硫原子而存在,由硒蛋白質P(Selenoprotein P)這個運輸蛋白所攜帶,而這個運輸形式在血漿中也佔了一半以上。其它類型的運輸形式還有甲硒氨酸(Selenomethionine),由硒原子取代原本在甲硫氨酸中的硫原子而存在,也是由硒蛋白質P所攜帶;除了這兩種有機硒之外,也有無機硒的運輸形式:硒酸鹽、亞硒酸鹽、硒化氢,與在人體血液中α球蛋白及β球蛋白的巯基( sulfhydryl groups)結合,例如:極低密度脂蛋白(VLDL)和低密度脂蛋白(LDL)。
而前述各種帶有硒且存在於血漿中的分子,均會被細胞所吸收。而細胞則釋放甲基化的硒化物至血漿中,再經由尿液將其排出體外。
- 分子特性
- 硒蛋白質P(Selenoprotein P)- 是一種含有硒半胱氨酸的血漿蛋白,也是一種運輸蛋白,主要是由肝臟合成,在血漿中大約有50%以上的硒是和含硒蛋白質P結合。含硒蛋白質P的結構最多可以帶有十個Sec殘基,當硒量下降時也會使殘基合成量下降。
- α球蛋白(α-globulin)- 其中又分成α 1-globulin及α 2-globulin。兩者均為醣蛋白,亦皆可幫助脂質的運輸。其中α 2-globulin又有一些不同的功能:幫助血紅素的運輸、銅運輸、血液凝集以及調控氧化酶的活性。
- β球蛋白(β-globulin)- 可以幫助脂質的運輸以及鐵和其他礦物質的運輸。
代謝
含硒胺基酸和無機態硒都會在組織中進行代謝。從飲食而來的甲硒胺酸其利用情形和甲硫胺酸相似,可儲存在胺基酸代謝池中,用於合成蛋白質,也可代謝成硒半胱氨酸和硒胱胺酸。
硒胺酸可以從飲食中直接得到,或是經由甲硒胺酸代謝而來。硒半胱氨酸經由β-硒半胱氨酸裂解酶作用之後產生游離態硒。游離態硒可以從谷胱甘肽(GSH)得到氫,然後生成硒化物(selenide)。硒化物有兩個代謝途徑,其一是經過甲基化作用後藉由尿液排出體外,或是形成硒代磷酸鹽(selenophosphate),這是體內重要含硒酵素的前驅物,例如5'-脫碘酶(5'-deiodinase)或榖胱甘肽過氧化酶(glutathione peroxidase)。
從食物中得來的硒酸鹽在體內可轉換成亞硒酸鹽,更進一步代謝成硒代谷胱甘肽(selenodiglutathione)及硒離子,後者成為硒蛋白或酵素的原料。
生化功能
硒最主要的功能是作為各種en:selenoprotein硒蛋白的組成分,進而影響其酵素活性或功能。
谷胱甘肽過氧化酶( glutathione peroxidase, GPX)
- 這是研究最多的含硒酵素,因為最早發現硒的生化功能就是作為谷胱甘肽過氧化酶的輔基。谷胱甘肽過氧化酶有五種亞型,通常標記為GPX1, 2, 3, 4, 5,每一種的亞型存在於不同的組織,但是催化相同的反應。主要的功能是消除組織中的過氧化氫(H2O2)和其他有機態過氧化物。還原過氧化物時,同時利用谷胱甘肽提供還原力(圖[12])。
甲狀腺素脫碘酶(Iodothyronine Deiodinases,IDI或DI)
- 脫碘酶是含硒蛋白質,酵素的活性區是硒半胱氨酸。已知有三種亞型。第一型存在肝臟、腎臟和肌肉,第二型及第三型存在皮膚、腦下垂體、脂肪細胞和腦。主要功能是催化甲狀腺素和相關代謝物脫去碘原子(圖),例如:5'-deiodinase(5'-DI)將T4型甲狀腺素脫碘轉換成T3型甲狀腺素,後者是體內活性最高的甲狀腺素,可調節代謝、生長及發育。去碘酶也會將T4轉換反式T3(reverse T3),催化產生反式T3的酵素是5-deiodinase。T3或是反式T3都可進一步脫碘產生T2或是3,3'-diiodothyronine,這些都是沒有活性的代謝物。
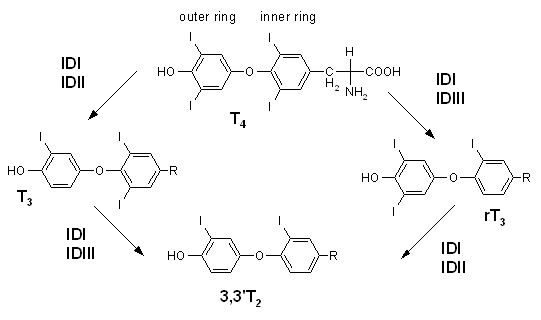 甲狀腺素脫碘酶的作用
甲狀腺素脫碘酶的作用
- 脫碘酶是含硒蛋白質,酵素的活性區是硒半胱氨酸。已知有三種亞型。第一型存在肝臟、腎臟和肌肉,第二型及第三型存在皮膚、腦下垂體、脂肪細胞和腦。主要功能是催化甲狀腺素和相關代謝物脫去碘原子(圖)
- 「硫氧化還原蛋白」還原酶(Thioredoxin Reductase,TrxR)
- 酵素的活性區有硒半胱氨酸,並含有FAD。此酵素存在血液、皮膚和肝臟等組織。主要反應是將氧化態的「硫氧化還原蛋白」(thioredoxin)中的雙硫鍵(disulfide bond)予以還原。還原態的「硫氧化還原蛋白」可以將氫原子提供給其他化合物(圖[13])。
- 硒代磷酸鹽合成酶(Selenophosphate Synthetase)
- 硒代磷酸鹽合成酶有兩種亞型,其中一型含硒半胱氨酸,催化硒離子磷酸化成硒代磷酸鹽的反應,這是合成含硒蛋白質的必備原料(圖[14])。
- 硒蛋白質P(Selenoprotein P)
- 這是硒的運輸蛋白質。有移除自由基的作用,具有抗氧化劑的功能。當體內的硒含量不足時,硒蛋白質P會優先獲得硒。
- 硒蛋白質W(Selenoprotein W)
- 含有硒半胱氨酸,主要存在心肌、骨骼肌和其它組織的細胞質中,可能扮演抗氧化劑的功能。
硒蛋白生合成分子機制
硒蛋白的硒胺酸是在轉譯過程合成並直接利用的,稱為轉譯插入反應(translational incorporation)。合成途徑需要的蛋白質有:硒胺酸合成酶selenocysteine synthase、硒半胱胺酸專用延長因子selenocysteine-specific elongation factor、selenocysteine-specific tRNA(tRNASec)、硒代磷酸鹽合成酶 selenophosphate synthetase。硒胺酸對應的基因密碼是UGA,此密碼通常當做終止密碼,但若配合mRNA序列3’端未轉譯區域具有獨特的二級結構SECIS(selenocysteine insertion sequence),則成為轉譯硒胺酸的密碼。
自然界中有許多細菌、植物或動物都能利用硒化氫(hydrogen selenide)合成多種有機化合物,如大蒜中的selenide garlic就是含有高單位的Se-methylselenocysteine。人類需要直接攝取有機的硒化物。自然界中甲硒胺酸(selenomethionine)插入硒蛋白質中是直接取代甲硫胺酸(methionine)的位置而得。也就是說在含甲硒胺酸的蛋白質合成過程是直接把甲硒胺酸當作甲硫胺酸編入,並沒有特殊密碼。人類再利用甲硒胺酸釋出的硒,先合成磷酸硒(selenophosphate)再生成硒半胱胺酸(selenocysteine, Sec)或其他小分子,再利用UGA的密碼將Sec編入人體的特殊蛋白硒蛋白質。人體硒的儲存者可能是硒蛋白質 P(selenoprotein p),在已被發現的14種硒蛋白質中只有硒蛋白質 P含有10到12個Sec,其Sec數可以隨血中硒的濃度而改變。其他的硒蛋白質都只有單一個Sec。所以硒帶蛋白質 P可能是人類硒的儲存池,當食物中硒供應不足時硒蛋白質 P就會釋出硒供人體利用,但是
至今仍無法證實其功能。
合成反應主要有四個步驟(圖示[15])
- 步驟一:tRNASec與Serine經由Seryl-tRNA synthetase作用,生成Seryl-tRNASec。
- 步驟二: 硒離子和ATP經由硒代磷酸鹽合成酶反應生成硒代磷酸鹽。
- 步驟三:Seryl-tRNASec和硒代磷酸鹽經由硒胺酸合成酶作用,產生含硒胺基酸殘基Selenocysteyl-tRNASec。
- 步驟四:轉譯時由SBP2和SECIS結合,繼而和tRNASec-eEFsec複合物結合,再與核醣體作用而誘導硒胺酸插入蛋白質(圖示[16])。
缺乏與毒性
缺乏症候群
- 動物缺硒
硒缺乏會引起牲畜類動物疾病。硒缺乏造成硒蛋白質酵素活性下降。若硒以外之營養狀況良好,硒缺乏僅造成輕微的臨床症狀。若伴有營養不良、化學藥物、感染等壓力,則會動物會出現嚴重病症。例如:硒缺乏加上維生素 E缺乏可導致大鼠與豬的之脂質過氧化與肝臟壞死,使豬、牛、羊的心臟損傷。在受感染的小鼠體內,硒缺乏可導致非致病性的coxsackie B3病毒轉變為具致病性的病毒,而造成小鼠的心肌炎。
- 人體缺硒
人體攝取不足時,會造成克山病和溪山症(Kashin-Beck disease)。
- 克山病的主要病癥為心肌病變(cardiomyopathy),包括心律加快、心電圖異樣、充血性心臟衰竭、心臟組織的多病灶壞疽等,嚴重時會導致生命危險甚至死亡。
- 克山症(Keshan disease)[17]是一種因為飲食缺乏微量元素硒所造成的充血性心肌病變症。此病症的命名來自於中国大陆北方的黑龙江省克山县,黑龙江省克山县是此病高流行的地區,發現是因為此地的土壤缺乏硒。克山症會造成心肌病變,好發於孩童和懷孕的婦女。補充硒可以改善病症,目前也發現此病症和病毒感染有關;特別是心肌病毒感染,如科薩奇病毒引起的心肌炎或感染過敏性心肌炎。本病的發生除了黑龍江省之外,在吉林、遼寧、內蒙古、河北、河南、山東、山西、陝西、甘肅、四川、雲南、西藏等地區都有病例,且病區多在荒僻山丘、高原及草原的農村,城鄉地區較少發病。
- 克山病的症狀主要是造成擴張性心肌病變(Dilated Cardiomyopathy)。心肌呈變形、壞死、和疤痕形成。心臟擴張腫大,多數左心室擴張比右心室嚴重。心臟的切面可以看到大小不等黃色、灰白色壞死、纖維化的疤痕;在顯微鏡下也可以觀察到心肌變性、肌纖維腫大、壞死的現象。適量的硒對缺硒造成的心肌損害有明顯的保護作用及抗氧化能力。硒是GSH-px的組成成分之一,該酶的主要作用是還原脂質過氧化物,清除自由基進而保護細胞膜的完整性。而低硒會造成GSH-px活性降低,造成心肌膜系統損傷。
- 克山症的臨床症狀主要為急性和慢性心功能不全、心臟擴大、心律不整以及腦、肺、腎等栓塞,根據1982年中華人民共和國全國克山病防治經驗交流會上的分形如下:
- 急性:突然發病的狀況,在中国大陆北方,急型病多發生在冬季,會因寒冷、過勞、感染、暴飲暴食或分娩等誘因而發病。重症者會出現心源性休克、急性肺水腫和嚴重心律失常的症狀。一開始可能感到頭暈、心窩部不適、反覆惡心嘔吐、吐黃水,繼而煩躁不安。嚴重者可在數小時或數天內死亡。患者常會面色蒼白,四肢冰冷,血壓降低,呼吸減慢。心臟一般輕度大,心音弱,尤其第一心音減弱,舒張期和收縮期會出現雜音。心律不整,主要為室性早搏、陣發性心動過速和房室傳導阻滯。急性心衰竭時肺部出現雜音,此外肝腫大和下肢水腫亦常見。
- 亞急型:發病不如急型快速。患者多為幼童,2~5歲佔85%。以春、夏季發病為多數。會出現心源性休克或充血性心力衰竭。發病初期表現為精神萎靡、咳嗽、呼吸急促、食欲不振、面色灰暗和全身水腫。亦會出現心臟擴大、奔馬律和肝腫大。腦、肺、腎等處的栓塞並不少見。
- 慢型:起病緩慢,很難被病患所察覺,亦可由急型、亞急型或潛在型轉化而來。臨床表現主要為慢性充血性心力衰竭,有心悸、呼吸急促,勞累後加重,並會有少尿、水腫和腹水。體檢觀察發現心臟向兩側明顯擴大,心音低,會聽到輕中度收縮期雜音和舒張期奔馬律,晚期可能出現右心衰竭的體徵如頸靜脈恕張、肝腫大和下肢浮腫等。嚴重者有胸、腹腔積液,心源性肝硬化等症狀。心律不整的症狀如室性早搏、心動過速、傳導阻滯、心房顫動等。
- 潛在型:可發生在平時看似健康的人,亦可為其他型好轉的階段。前者常無症狀,可照常勞動或工作,而在普查中被發現,此屬穩定的潛在型。由其他型轉變而來者可有心悸、呼吸急促、頭昏、無力等症狀。心電圖會有ST-T變化,QT間期延長和過早搏動。潛在型心臟雖受損,但心功能代償良好。心臟不增大或輕度增大。
- 克山症的預防措施首應注意環境衛生和個人衛生。保護水源,改善水質。改善營養條件,防止偏食,尤其對孕婦、產婦和兒童更應加強補充蛋白質,各種維生素及人體必需的微量元素,包括鎂、碘等,並防治大骨節病、地方性甲狀腺病。 且流行區推廣預防性服藥 採用硒酸鈉作為預防性服藥,經多年推廣,證明可明顯降低發病率。通常採用每10天口服一次,1~5歲1mg,6~10歲2mg,11~15歲3mg,16歲以上4mg。非發病季節可停服三個月。此外,流行區推薦使用含硒食鹽。農村使用含硒液浸過的種子種植。植物根部施加含硒肥料以提高農作物中含硒量。
- 溪山症的主要病徵為骨關節病變(osteoarthropathy),包含骨關節、小腿、手臂的軟骨骺版退化與壞死。此疾病為地域性、多發性、變形性骨關節病變,出現於亞洲低硒地區青春期前兒童與青少年。上述症狀僅發生於硒缺乏者,但改善硒營養狀況並無法完全避免此疾病。
- 兒童和全靜脈營養病人發生硒缺乏時,易導致關節僵硬、肌肉痛、頭髮和皮膚失去色素顏色、生長遲滯、指甲白化等症狀。生長遲滯的現象與硒在甲狀腺素的代謝有關。
毒性
- 化合物形式與毒性
元素態的硒和大部分的金屬硒化物毒性較小,因為生物可用性(bioavailability)小。硒酸鹽和亞硒酸鹽的毒性較大,硒化氫(hydrogen selenide)的毒性最大,是一種氣狀的硒化合物。有機態硒化物如甲硒胺酸和硒胺酸與含硫胺基酸相似,因此毒性較無機態硒為低,但其吸收率高,雖不致造成急性毒害,但長期大量攝取,會產生與無機硒相似的中毒症狀。
硒中毒(selenosis)可能發生在工人以及攝取過多硒的族群。目前訂定硒的上限攝取量為每天400μg;硒的副作用發生最低量(LOAEL)為910 μg。攝食過量時,極易導致毛髮異樣、指甲脫落、腳趾甲異樣等副作用,不過並無飲食硒中毒的案例。
中毒的嚴重程度與所攝取的硒含量成正比的關係。中毒的症狀包含:反胃嘔吐、疲勞、腹瀉、頭髮與指甲損壞、異常刺痛感等,也會干擾硫的正常代謝以及抑制蛋白質合成。服用含有高量硒的藥物會造成急性硒中毒,嚴重過量會導致肝硬化, 肺水腫(pulmonary edema),甚至喪命。治療硒在體內不平衡所造成的症狀目標:1.降低關節炎症狀;2.降低血壓;3.改善皮膚、毛髮及指(趾)甲問題。
食物硒含量取決於土壤硒含量。美國雖有高硒地區,但農業部(USDA)已確認這些地區,並禁止飼養動物作為食物來源。美加地區食物運銷系統發達,可確保個人不會只攝食到當地農產,保障民眾硒攝取量不致過高或過低。
- 硒中毒的生化指標
硒蛋白質含量在硒需要量達到後,即呈現飽和狀態,不再隨硒攝取量增加而上升,因此無法被用於評估硒的毒性。測量組織(血液、血漿)的硒含量有助於評估硒中毒的危險性。尿液硒排除量在特定控制之條件下,可作為硒毒性的指標。臨床症狀如毛髮、指甲易碎裂脫落等常被報導,是主要的評估終點。硒的甲基化代謝物因測量誤差大,且受許多因素影響,不適用於硒中毒指標。
與其他營養素的關係
體內含鉛量增多時會有硒濃度下降的現象。銅不足會降低榖胱甘肽過氧化酶和5'-脫碘酶的活性。硒與甲硫胺酸的利用有關。從食物攝取的硒有一部分是甲硒胺酸的形式,可作為合成蛋白質的材料。當甲硫胺酸供應不足時,甲硒胺酸會成為它的替代物而用在蛋白質的合成,而不會代謝成為硒離子以供利用,間接引發硒的不足。鐵的缺乏會減少榖胱甘肽過氧化酶的合成,減少組織中的硒濃度。維生素E和榖胱甘肽過氧化酶同樣有抗氧化的功能,在使細胞膜和DNA免於自由基的攻擊機制上,硒和維生素E常一起作用,在功能上也有互補作用,其中一者濃度較高會減低另一濃度較低者所造成的影響[18]。
有機硒化學
硒,特别是在II氧化态的硒与碳形成稳定的键,其结构类似于相应的有机硫化合物。硒和硫有類似的性質,因此,許多有機硫化合物都有硒的版本。
硒醇
硒醇和醇類一樣有易揮發性,和硫醇同樣有異味,且醇類都會有硒醇衍生物,如正丁醇的衍生物為正丁硒醇,硫醇亦然,如乙硫醇的衍生物為乙硒醇。
硒醚
参阅
- 地球的地殼元素豐度列表
- 塞勒涅
参考文献
^ 1.01.11.2 《化学元素反应手册》. P528. 第三节 硒
^ Gropper SS, Groff JL, et al. (2005)Advanced Nutrition and Human Metabolism, 4th ed., pp. 456-461. Wardswirth, ISBN 0-534-55986-7
^ Gordon M. Wardlaw, Jeffery S. Hampl Perspectives in Nutrition, 7th edition, P.422
^ 行政院衛生署(2003)國人膳食營養素參考攝取量及其說明,修訂第六版,pp. 422-447。台灣行政院衛生署,ISBN 957-01-4677-X
^ Institute of Medicine (2000) Dietary Reference Intakes for Vitamin C, Vitamin E, Selenium, and Carotenoids, pp. 284-324. National Academy Press, ISBN 0-309-06949-1
^ Institute of Medicine (2000) Dietary Reference Intakes for Vitamin C, Vitamin E, Selenium, and Carotenoids, pp. 284-324. National Academy Press, ISBN 0-309-06949-1
^ 行政院衛生署(2003)國人膳食營養素參考攝取量及其說明,修訂第六版,pp. 422-447。台灣行政院衛生署,ISBN 957-01-4677-X
^ Institute of Medicine (2000) Dietary Reference Intakes for Vitamin C, Vitamin E, Selenium, and Carotenoids, pp. 284-324. National Academy Press, ISBN 0-309-06949-1
^ 行政院衛生署(2003)國人膳食營養素參考攝取量及其說明,修訂第六版,pp. 422-447。台灣行政院衛生署,ISBN 957-01-4677-X
^ http://www.vitaminherbuniversity.com/topic.asp?categoryid=2&topicid=1028
^ http://www.lammd.com/opinion/selenium_and_vitamin_C_absorption.cfm
^ 存档副本. [2008-01-10]. (原始内容存档于2010-06-03).
^ 存档副本. [2008-01-10]. (原始内容存档于2005-04-09).
^ http://dir.nhlbi.nih.gov/labs/lb/images/Perselenide.jpg
^ http://www.freepatentsonline.com/20050048548-0-large.jpg
^ http://www.nature.com/ng/journal/v37/n11/images/ng1105-1162-F1.gif
^ 新華網www.xinhuanet.com
^ Gropper SS, Groff JL, et al. Advanced Nutrition and Human Metabolism, 5th ed., pp. 511,318.
外部链接
维基共享资源中相关的多媒体资源:硒 |
| 查询維基詞典中的selenium。 |
Selenium at The Periodic Table of Videos (University of Nottingham)- National Institutes of Health page on Selenium
- Assay
- ATSDR – Toxicological Profile: Selenium
- CDC - NIOSH Pocket Guide to Chemical Hazards
- Peter van der Krogt elements site
*氧族元素 | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| | IA 1 | IIA 2 | IIIB 3 | IVB 4 | VB 5 | VIB 6 | VIIB 7 | VIIIB 8 | VIIIB 9 | VIIIB 10 | IB 11 | IIB 12 | IIIA 13 | IVA 14 | VA 15 | VIA 16 | VIIA 17 | VIIIA 18 | ||||||||||||||||||
1 | H | | He | |||||||||||||||||||||||||||||||||
2 | Li | Be | | B | C | N | O | F | Ne | |||||||||||||||||||||||||||
3 | Na | Mg | | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||
4 | K | Ca | | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||
5 | Rb | Sr | | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||
6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||
7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||
| ||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||
|
