顺反异构

Multi tool use

顺-2-丁烯

反式-2-丁烯
顺反异构(英语:cis-trans isomerism),舊称几何异构[1],是存在于某些双键化合物或环状化合物中的一种立体异构现象。由于存在双键或环,这些分子的自由旋转受阻,产生两个物理性質或化學性質均不相同的同分异构体,分别称为顺式(cis)和反式(trans)异构体。
“顺式加成”指的是从双键/三键的同一侧进行加成反应;“反式加成”指的是从双键/三键的两侧进行加成。
在双键化合物中,若与两个双键原子相连的相同或相似的基团处在双键的同侧,则该化合物被称为“顺式”异构体;若两个基团处于异侧,则定义为“反式”异构体,比如右图所示的2-丁烯的两个同分异构体。
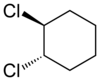
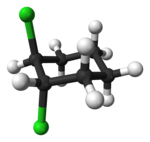
在环状化合物中,若两个相同的取代基位于环平面的同侧,则称该化合物为“顺式”;反之称为“反式”。例如下图的1,2-二氯环己烷的两个异构体:
  |
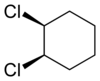  |
| 反-1,2-二氯环己烷 | 顺-1,2-二氯环己烷 |
由于顺式与反式异构体中原子的空间排列不同,它们的物理性质[2](如熔点[3]、沸点[4]、溶解度)和化学性质通常也有不同。一般来说,反式异构体比顺式异构体稳定。这是因为顺式异构体中两个相同基团处于同侧,可能造成偶极矩的叠加,增加不对称性,而反式异构体中两个基团以双键中心形成中心对称,所造成的影响可以相互抵消。但以上规则也不是绝对的,比如在有些1,2-二卤乙烯、1,2-二氟二氮烯(FN=NF)中,顺式异构体便比反式稳定[5]。这种顺式比反式异构体稳定的现象被称为“顺式效应”(cis效应)[6]。
目录
1 物理性質的比較
2 E/Z标记
3 参见
4 参考资料
物理性質的比較
順式和反式異構體通常具有不同的物理性質。在一般情況下,造成同分異構體之間的差異,是因為分子的排列或整體偶極矩的改變。
 |
 |
| 順-2-戊烯 | 反-2-戊烯 |
 |
 |
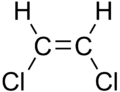
| 順-1,2-二氯乙烯 | 反-1,2-二氯乙烯 |
 |
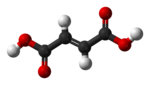 |
| 順丁烯二酸 (maleic acid) |
反丁烯二酸 (fumaric acid) |
 |
 |
| 順式油酸 | 反式油酸 |
这些差異其實很微小,如直鏈的烯烴,舉例來說 2 - 戊烯,在37℃時為順式異構物;36℃下為反式異構物。[7] 但是如果出現極性鍵,順式和反式異構體之間的差異會比較大的,如1,2-二氯乙烯,順式異構物的沸點為60.3℃,而反式異構物的沸點為47.5℃。[8] 順式異構體中兩極C-Cl鍵的偶極矩相結合,使整體分子具偶極性,以致於具有偶極-偶極力使得倫敦色散力增加和提高沸點;另一方面在反式異構物中則不會發生,因為兩極C-Cl鍵的偶極矩沒有結合,使其偶極矩為零。
丁烯二酸的兩種異構體性質與反應活性差異較大,順式異構體被稱為順丁烯二酸;反式異構體為反丁烯二酸。造成沸點差異的關鍵為極性,因為它會導致分子間作用力增加,進而提高沸點。
同樣,造成 熔點差異的關鍵為結構之對稱性,例如油酸,順式異構物熔點為13.4度在室溫下為液體;反式異構物具有高熔點43度在室溫下是固體。因此,反式烯烴因為極性較小或對稱性佳有較低的沸點和較高的熔點;反之,順式烯烴因為具極性和對稱性不佳有較高的沸點和較低的熔點。
因為反式烯烴比順式烯烴更具對稱性,所以反式烯烴往往有更高的熔點以及在惰性溶劑中的溶解度較低[9]。
核磁共振光譜測量鄰位的偶合常數(3JHH),反式異構物(範圍:12–18 Hz;典型:15 Hz)大於順式異構物(範圍:0–12 Hz;典型:8 Hz)[10]。
E/Z标记

根据顺序规则,溴的原子序数大于氯,比氯优先。因此上面的化合物为Z型异构体。
对双键化合物的顺反标记法对双键原子所连有的基团是有严格要求的,不适用于雙鍵二端所连四個基团不相同时的情况,有很多缺点。因此,就要使用另一套命名双键化合物的规则—E/Z标记法。Z来源于德语的“zusammen”,意为“在一起”,与cis-相当;E来源于德语的“entgegen”,意为“相反”,与trans-相当。
在使用E/Z标记时,首先要根据顺序规则确定每个双键原子所连两个基团的优先顺序。若两个双键原子所连的较优先的基团处在双键同侧,则称之为“Z-异构体”;反之则称为“E-异构体”。
顺反标记法和E/Z标记是兩套獨立的標記系統,一般來說Z-异构体相當於順式异构体,E-异构体相當於反式异构体,不過也有例外。
参见
- 异构体
- 结构异构
- 手性
- 反式脂肪
参考资料
^ 几何异构是IUPAC不推荐的名称,参见其对“几何异构”的定义。
^ Advanced organic Chemistry, Reactions, mechanisms and structure 3ed. page 111 Jerry March ISBN 0-471-85472-7
^ Alkene Compound Boiling Points. www.chemicalland21.com. [2018-07-18].
^ Cope, Arthur C; Bach, Robert D. (1969). "trans-cyclooctene". Org. Synth. 49: 39; Coll. Vol. 5: 315.
^ The stereochemical consequences of electron delocalization in extended .pi. systems. An interpretation of the cis effect exhibited by 1,2-disubstituted ethylenes and related phenomena Richard C. Bingham J. Am. Chem. Soc.; 1976; 98(2); 535-540 Abstract
^ Contribution to the Study of the Gauche Effect. The Complete Structure of the Anti Rotamer of 1,2-Difluoroethane Norman C. Craig et al. J. Am. Chem. Soc.; 1997; 119 p 4789 doi:10.1021/ja963819e
^ Chemicalland values. Chemicalland21.com. [2010-06-22].
^ CRC Handbook of Chemistry and Physics, 60th Edition (1979-80), p.C-298
^ Advanced organic Chemistry, Reactions, mechanisms and structure 3ed. page 111 Jerry March ISBN 0-471-85472-7
^ "Spectroscopic Methods in Organic Chemistry," Dudley H. Williams and Ian Fleming, 4th ed. revised, McGraw-Hill Book Company (UK) Limited, 1989.Table 3.27
|
0VsKSAzVF YIZ,Zihq Mx8sv,B8Xn9udzUxIOPmdK6TH3DqHumU8GcBAFdooYWSqy94lQ