氢氧化钾
| 氢氧化钾 | |
|---|---|
 | |
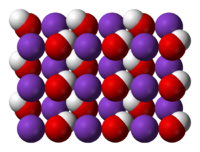 | |
| 英文名 | Potassium hydroxide |
| 别名 | 苛性钾 |
| 识别 | |
CAS号 | 1310-58-3 |
PubChem | 14797 |
ChemSpider | 14113 |
SMILES |
|
InChI |
|
InChIKey | KWYUFKZDYYNOTN-REWHXWOFAT |
UN编号 | 1813 |
EINECS | 215-181-3 |
ChEBI | 32035 |
RTECS | TT2100000 |
| 性质 | |
化学式 | KOH |
摩尔质量 | 56.10564 g·mol⁻¹ |
| 外观 | 白色潮解固体 |
密度 | 2.044 g/cm3 |
熔点 | 360.4℃[1] |
沸点 | 1327℃ |
溶解性(水) | 1100 g/L |
pKb | -1.1 (KOH(aq) = K+ + OH–) [2] |
| 结构 | |
晶体结构 | 单斜 |
| 危险性 | |
欧盟危险性符号  腐蚀性 C 腐蚀性 C | |
警示术语 | R:R22-R35 |
安全术语 | S:S1/2-S26-S36/37/39-S45 |
NFPA 704 |  0 3 1 ALK |
闪点 | 不可燃 |
| 相关物质 | |
| 其他阴离子 | 氧化钾,过氧化钾,超氧化钾 |
| 其他阳离子 | 氫氧化鋰 氫氧化鈉 氫氧化銣 氫氧化銫 氫氧化鍅 |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
氢氧化钾(化学式:KOH),俗稱苛性鉀,白色固体,溶于水、醇,但不溶于醚。在空气中极易吸湿而潮解。可与二氧化碳反应生成碳酸钾。所以它會被用作吸收二氧化碳之用。
氢氧化钾是典型的強鹼,有許多工業上的應用,大部份的應用都是因為氢氧化钾可以和酸反應,以及氢氧化钾本身的腐蝕性。2005年生產的氢氧化钾估計有700,000至 800,000噸,約為氢氧化鈉的百分之一[3]。氢氧化钾常用來製造軟肥皂和液體肥皂,也用來製備含鉀的化學物質。
目录
1 制备
2 物理性质
3 安全性
4 用途
5 参考资料
制备
可從電解飽和的氯化鉀水溶液製得。
- 2 KCl + 2 H2O → 2 KOH + Cl2↑ + H2↑
古法會用碳酸钙加熱,再和水及草木灰反應,生成氢氧化钾。
先將碳酸钙高温加热碳酸钙生成氧化钙
- CaCO3====CaO+CO2↑{displaystyle {rm {CaCO_{3}{=!=!=!=}CaO+CO_{2}uparrow }}}
再將氧化钙与水反应生成氢氧化钙
- CaO + H2O → Ca(OH)2
最後將氢氧化钙与草木灰反应生成氢氧化钾
- Ca(OH)2 + K2CO3 → CaCO3↓ + 2KOH
事實上,水与鉀反應也會生成氫氧化鉀,但反應十分劇烈,不宜使用:
- 2K+2H2O====2KOH+H2↑{displaystyle {rm {2K+2H_{2}O{=!=!=!=}2KOH+H_{2}uparrow }}}
物理性质
氢氧化钾是白色吸湿性固体,高于熔点极易升华。[1] 极易溶于水和乙醇。固體氫氧化鉀為白色正交結晶,市售品有塊狀、小颗粒状和片狀。
安全性
有强烈腐蚀性,溶於水放出大量熱。吸入后强烈刺激呼吸道或造成灼伤。皮肤和眼直接接触可引起灼伤,一旦眼睛或皮膚接觸到氫氧化鉀,迅速將受傷部位以水不斷沖洗15 分鐘以上;口服會灼伤消化道,可致命。
用途
氢氧化钾用作生產鉀鹽,如高錳酸鉀、亞硝酸鉀、磷酸氫二鉀等。日化工業用作製造肥皂。電池工業用於製造鹼性電池的電解質。
参考资料
^ 1.01.1 《无机化合物制备手册》.朱文祥 主编. 化学工业出版社. P21. 【Ⅰ-47】氢氧化钾(potassium hydroxide)
^ Sortierte Liste: pKb-Werte, nach Ordnungszahl sortiert. – Das Periodensystem online.
^ H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger “Potassium Compounds” in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. doi:10.1002/14356007.a22_039
| ||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|

